Χορήγηση Μεσεγχυματικών Βλαστοκυττάρων στο Μεσοσπονδύλιο Δίσκο και στις Σπονδυλικές Διαρθρώσεις
Χορήγηση Μεσεγχυματικών Βλαστοκυττάρων στο Μεσοσπονδύλιο Δίσκο και στις Σπονδυλικές Διαρθρώσεις
Γιώργος Σάπκας
Καθηγητής Ορθοπαιδικής Πανεπιστημίου Αθηνών
Εισαγωγή
Τα τελευταία χρόνια γίνονται μεγάλες προσπάθειες να αντιμετωπισθεί το μείζον κοινωνικό και οικονομικό πρόβλημα που απορρέει από την εκφύλιση των Μεσοσπονδύλιων Δίσκων και των Σπονδυλικών Διαρθρώσεων, δια της εφαρμογής κυτταρικής θεραπείας.
Πλείστες πειραματικές μελέτες έχουν γίνει σε πειραματόζωα και πλέον πραγματοποιούνται κλινικές μελέτες και εφαρμογές κυτταρικών θεραπειών σε ανθρώπους, δηλαδή, γίνεται έγχυση Μεσεγχυματικών Βλαστοκυττάρων τα οποία λαμβάνονται από τον ίδιο τον πάσχοντα, στους εκφυλισμένους Μεσοσπονδύλιους Δίσκους και στις Σπονδυλικές Διαρθρώσεις (Facets).
Είναι φυσικό να υπάρχουν αντίθετες ή και αλληλοσυγκρουόμενες απόψεις σε όλες τις θεραπείες, όσον αφορά τις ενδείξεις, την αποτελεσματικότητα, τις πιθανές επιπλοκές και πλήθος άλλων παραμέτρων.
Ασφαλώς, είναι πολύ ενωρίς να καταλήξουμε σε συμπεράσματα, δεδομένου ότι υπάρχουν πολλές και αντίθετες απόψεις επί αυτού του θέματος. Δια το λόγο αυτό, παρατίθεται η πλέον σύγχρονη Διεθνής Βιβλιογραφία, ώστε να δοθεί μια έγκυρη πληροφόρηση.
Άρθρο των Pettine Κenneth et al, (2015)
Πολύ ενδιαφέρουσα είναι η δημοσίευση των Pettine Kenneth et al, (1) η οποία αναφέρεται στη θεραπεία της Οσφυαλγίας που οφείλεται σε εκφύλιση των Μεσοσπονδυλίων Δίσκων (ΜΔ) δια της εγχύσεως αυτόλογου συμπυκνώματος μυελού των οστών μέσα στους Μεσοσπονδύλιους Δίσκους, σε 26 ασθενείς που παρακολουθήθηκαν για περίοδο δύο χρόνων. Η ηλικία των ασθενών κυμαινόταν από 18 μέχρι 61 ετών (Μέσος όρος 40 έτη) και ήσαν 11 άνδρες και 15 γυναίκες με Μέσο Βάρος ΒΜΙ 26,6 (19-37).
Η θεωρητική βάση της μελέτης απευθύνεται στις πηγές εκφύλισης του Μεσοσπονδύλιου Δίσκου (ΜΔ), επηρεάζοντας τη φλεγμονή του Πηκτοειδούς Πυρήνα (ΠΠ) του Μεσοσπονδύλιου Δίσκου ή την εκφύλιση του Ινώδους Δακτυλίου (ΙΔ), την επανυδάτωση του πυρήνα δια της ανακατασκευής (Remodeling) του ιστού, ή επανα-συγκέντρωσης περιφερικών κυττάρων, θρεπτικών ουσιών ή αιμοφόρων αγγείων και/ή με την αποκατάσταση του ύψους του Μεσοσπονδυλίου Δίσκου, μειώνοντας κατ’αυτό τον τρόπο τη πίεση στα παρακείμενα νεύρα.
Χρησιμοποιώντας παρασκευάσματα αυτόλογων Πρόδρομων Κυττάρων τα οποία περιλαμβάνουν Μεσεγχυματικά Βλαστοκύτταρα (MSCs) που βρίσκονται σε συμπύκνωμα οστικού μυελού (Bone Marrow Concentrate-BMC), τίθεται το ερώτημα αν μπορεί να υπάρξει θεραπευτική αντιμετώπιση διαφορετική από τις υπάρχουσες συντηρητικές ή χειρουργικές θεραπείες (11,12).
Η μελέτη των Pettine Kenneth et al, (1) ήταν προοπτική, όχι τυχοποιημένη και έγινε σε ένα μόνο Κέντρο από τους συγγραφείς. Οι ασθενείς που περιελήφθησαν στη μελέτη είχαν μέτρια έως σοβαρά συμπτώματα Οσφυαλγίας, δισκογενούς αιτιολογίας. Τα συμπτώματα υφίσταντο ήδη 6 μήνες, είχαν υποβληθεί ανεπιτυχώς σε συντηρητική θεραπεία και είχε γίνει ακτινολογική διερεύνηση με Μαγνητική Τομογραφία. Το Pfirrmann Score κυμαινόταν από 4 έως 7, το στάδιο Modic ήταν ΙΙ ή λιγότερο, η απώλεια ύψους του ΜΔ ήταν 30% περίπου συγκρινόμενο προς το παρακείμενο φυσιολογικό ΜΔ, το Oswestry Disability Index (ODI) ήταν τουλάχιστον 30 στη κλίμακα 100 και το VAS (Visual Analogue Score) τουλάχιστον 40 mm στη κλίμακα 100 mm. Εξαιρούντο της μελέτης ασθενείς με νευρολογικές διαταραχές στα κάτω άκρα, με συμπτωματολογία Σπονδυλικής Στένωσης, Κήλης του Μεσοσπονδυλίου Δίσκου, με Σπονδυλόλυση ή και με Σπονδυλολίσθηση. Οι ασθενείς ελέγχθηκαν κλινικά και υποβλήθηκαν στους ελέγχους ODI και VAS, στους 3,6,12 και 24 μήνες μετά την έγχυση.
Από τους 26 ασθενείς, ενδοδισκική έγχυση αυτόλογου BMC έγινε σε ένα συμπτωματικό Μεσοσπονδύλιο Δίσκο (ΜΔ) και σε άλλους 13 σε δύο συμπτωματικούς παρακείμενους ΜΔ. Σε όλους τους ασθενείς οι εγχύσεις έγιναν σε ΜΔ, βάσει των ευρημάτων της MRI. Τα MRI επαναλήφθηκαν στους 12 μήνες. Το Phirrmann Score καθορίσθηκε από ανεξάρτητο ερευνητή.
Η αναρρόφηση του Οστικού Μυελού (BMA-Bone Marrow Aspirate) έγινε από την οπίσθια άνω λαγόνιο ακρολοφία του ασθενούς και οι σύριγγες είχαν αντιπηκτικό. H αναρρόφηση έγινε υπό τοπική αναισθησία, χρησιμοποιώντας το ειδικό Trocar Jamshidi. Η ποσότητα του αναρροφηθέντος ΒΜΑ ήταν περίπου 60 ml βάσει της τεχνικής που συνεστήθη υπό των Hernigou et al, (13).
Περαιτέρω το ΒΜΑ υποβλήθηκε σε ειδική επεξεργασία δια διαδικασίας η οποία παρέχεται από το ART Bone Marrow Concentration System, ώστε να ληφθεί η επιθυμητή ποσότητα συμπυκνωμένων κυττάρων του οστικού μυελού (Bone Marrow Concentrated Cell preparation).
Η κυτταρική ανάλυση του παρασκευάσματος των περιεχομένων Εμπύρηνων κυττάρων (Total Nucleated Cell-TNC-Concentration) κυμαινόταν από 50.000 μέχρι 1 εκατομμύριο per well σε 12 well plates, τυπικά, όγκος 7 ml.
Το BMC χορηγείτο υποδορίως μέσα στο προβληματικό Μεσοσπονδύλιο Δίσκο, με βελόνα 22 gauge. Περίπου 2-3 ml κ.εκ. BMC χρησιμοποιήθηκαν για κάθε συμπτωματικό επίπεδο. Στους ασθενείς χορηγούντο αναλγητικά για το πόνο για τρείς ημέρες και τους δίδονταν οδηγίες να περιορίσουν τις φυσικές δραστηριότητες για δύο εβδομάδες.
Επί τη βάσει των ικανοποιητικών αποτελεσμάτων που διαπίστωσαν στη σειρά των 26 ασθενών, τους οποίους παρακολούθησαν για τουλάχιστον 2 χρόνια, οι Pettine et al (1), προέβησαν σε ορισμένες παρατηρήσεις.
1. Οι βιολογικές θεραπείες για τη θεραπεία του δισκογενούς πόνου είναι ελκυστικές, διότι είναι πολύ λίγο επεμβατικές και κοστίζουν λιγότερο από τις χειρουργικές επεμβάσεις.
2. Οιαδήποτε προετοιμασία-παρασκευή κυττάρων η οποία δεν ανταποκρίνεται στις οδηγίες που έχουν δοθεί από τον οργανισμό FDA (Food and Drug Administration) των ΗΠΑ, οδηγίες του Τμήματος 61 (Section 61),- (η διαδικασία πρέπει να είναι με αυτόλογα κύτταρα, που να έχουν υποβληθεί σε ελάχιστους χειρισμούς, να είναι μία η επέμβαση κτλ.)- κατηγοριοποιείται σαν φάρμακο (ή 351 προϊόν) και δεν επιτρέπεται επί του παρόντος να δίδονται εκτός ειδικών κλινικών δοκιμασιών με άδεια.
Αυτό περιλαμβάνει τα αλλογενή κύτταρα, in vitro καλλιέργεια κυττάρων, με ένζυμα ή υπερήχους διασπώμενα κύτταρα του λιπώδους ιστού, ή στρωματικά ενδοθηλιακά κύτταρα αγγείων, οστικό μυελό πτωμάτων και προϊόντα από τον πλακούντα και amniotic.
3. To Platelet-Rich Plasma (PRP) , δίδει αυτόλογους αυξητικούς παράγοντες για αναγεννητικές εφαρμογές και μπορεί να παραχθεί δια διαφόρων συσκευών που έχουν πάρει έγκριση από το FDA, όμως το PRP δεν παρέχει πρόδρομα πολυδύναμα (progenitor cells) Μεσεγχυματικά Βλαστοκύτταρα (Stem Cells) όπως παράγονται από το πλήρες αίμα (27).
4. Δεδομένου ότι ο ΜΔ είναι ένας ανάγγειος ή ελάχιστα αγγειούμενος ιστός, θεωρείται ότι οποιοδήποτε βιολογικό υλικό ενεθεί στο ΜΔ θα πρέπει να περιέχει πρόδρομα Πολυδύναμα κύτταρα (progenitor cells), για να συμμετάσχει στην επουλωτική διαδικασία είτε άμεσα είτε μέσω των παρακρινών δράσεων (11). Το αυτόλογο BMC συμπυκνωμένο σε βαθμό δραστικότητας, προσδιορίσθηκε από το FDA σαν συμπληρωματική πηγή πολυδύναμων Μεσεγχυματικών Βλαστοκυττάρων για τη θεραπεία του δισκογενούς πόνου.
5. Το μέγεθος και η διάρκεια της ανακούφισης από το πόνο και γενικότερα τα κλινικο-ακτινολογικά αποτελέσματα με τη πυκνότητα-αριθμό των εγχεόμενων Μεσεγχυματικών Βλαστοκυττάρων (CFU-F/MSC),δεν μπορεί να προκαθορισθεί.
6. Oι Pettine et al, είχαν ήδη δημοσιεύσει τα αποτελέσματα της ίδιας σειράς ασθενών, με διάρκεια παρακολούθησης 12 μήνες (28). Τότε είχαν διαπιστώσει ότι η κατά μέσο όρο μέση μείωση της ανικανότητας εκτιμούμενης με το ODI Τest ήταν 58% και η μέση μείωση του πόνου με το VAS Test ήταν 61%. Η μεγαλύτερη βελτίωση συνέβη μέσα στους τρείς πρώτους μήνες μετά την έγχυση και διατηρήθηκε μέχρι και τους 12 μήνες. Η συγκέντρωση/ποσό των Μεσεγχυματικών Βλαστοκυττάρων, συσχετιζόταν με τη βελτίωση του πόνου και της ανικανότητας.
Οι ασθενείς, στους οποίους ο αριθμός των Μεσεγχυματικών Βλαστοκυττάρων ήταν μεγαλύτερος από 2000 ανά κ.εκ. (2000 MSC/ml), είχαν 70% μείωση του ODI και 69% μείωση του VAS. Μόνο 2 από τους 26 ασθενείς, υποβλήθηκαν τελικά σε χειρουργική επέμβαση 6 με 12 μήνες μετά τις εγχύσεις. Όσον αφορά τον έλεγχο με το MRI (29) που είναι αντικειμενική μέθοδος εξέτασης, ενώ οι άλλες έχουν έντονα υποκειμενικό χαρακτήρα, παρατηρήθηκε ότι σε 8 από τους 12 ασθενείς, στο MRI των 12 μηνών, υπήρξε βελτίωση τουλάχιστον κατά μία κλίμακα Phirrmann.
7. Στη τρέχουσα μελέτη τους, με παρακολούθηση 24 μηνών, οι Pettine et al, (1) διαπίστωσαν ότι υπάρχει διάρκεια στη βελτίωση του πόνου και της ανικανότητας. Τα αποτελέσματα είναι καλύτερα αξιοσημείωτα συγκρινόμενα με εκείνα άλλων θεραπειών και χειρουργικών επεμβάσεων (7). Στα 2 χρόνια παρακολούθησης, μόνο 5 από τους 26 ασθενείς υποβλήθηκαν σε χειρουργική επέμβαση και από αυτούς μόνον ο ένας είχε σημαντική βελτίωση του πόνου και της ανικανότητάς του.
Οι υπόλοιποι 21 ασθενείς βελτιώθηκαν τόσο ώστε κανένας από αυτούς δεν ζήτησε να υποβληθεί σε χειρουργική επέμβαση. Κανένας από τους ασθενείς δεν έγινε χειρότερα από την έγχυση των Μεσεγχυματικών Βλαστοκυττάρων (ΒMC) και δεν υπήρξαν ουσιώδεις επιπλοκές στη χειρουργική διαδικασία. Συνολικά η πλειοψηφία των ασθενών που περιελήφθησαν στη μελέτη, έδειξε να υπάρχει σταθερή και διαρκής βελτίωση των κλινικών παραμέτρων ODI και VAS, μετά από μία και μόνο έγχυση BMC στο Μεσοσπονδύλιο Δίσκο.
8. Η απουσία αντιδραστικών διαδικασιών-παρενεργειών κατά τη δίχρονη παρακολούθηση των ασθενών, είτε κατά τη διαδικασία αναρρόφησης οστικού μυελού από τη λαγόνιο ακρολοφία της πυέλου, είτε κατά την ενδο-δισκική έγχυση των Μεσεγχυματικών Βλαστοκυττάρων του Μυελού των Οστών (BMC), παρέχει ισχυρή υποστήριξη στη δυνατότητα κλινικής εφαρμογής χρησιμοποιήσεως αυτόλογων BMC, για τη θεραπεία ασθενών με εκφύλιση του Μεσοσπονδυλίου Δίσκου (DDD).
Η αναφερθείσα συσχέτιση του βαθμού διαρκείας/μείωσης του VAS και του ODI, σε ασθενείς στους οποίους το ενέσιμο ήταν μεγαλύτερο σε αριθμό Μεσεγχυματικών Βλαστοκυττάρων από 2000 ανά κ.εκ. (C>2000 MSC/ml), τονίζει την ανάγκη να παρέχεται ΒΜC με μεγαλύτερη συγκέντρωση (concentration) μονοπυρηνικών κυττάρων, περιλαμβάνοντας πρόδρομα κύτταρα, όπως τα MSCs.
9. Αυτά τα προκαταρκτικά αποτελέσματα υποστηρίζουν ισχυρά την ενδοδισκική έγχυση αυτόλογων BMC στο παθολογικό Μεσοσπονδύλιο Δίσκο, για τη θεραπεία δισκογενούς πόνου, αφού έχει αποτύχει η συντηρητική αγωγή προτού να γίνει χειρουργική επέμβαση. Το κόστος της επέμβασης συνολικά είναι πολύ μικρότερο των άλλων θεραπειών και πραγματοποιείται υπό τοπική αναισθησία με/ή χωρίς μέθη και ο ασθενής εξέρχεται αυθημερόν του Νοσοκομείου.
References
1. Pettine Kenneth et al,: Treatment of Discogenic Back Pain with Autologous Βone Marrow Concetrate Injection with minimum two years follow-up. International Orthopaedics (SICOT) 2015,p.264-270. 2. Phillips FM, Slosar Pj, Youssef JA et al, (2013) Lumbar Spine Fusion for Chronic Low Back Pain due to Degenerative Disc Disease: a systematic review. Spine(Phila.Pa 1976)38:E409-E-422.doi.10.1097/BRS0b0 13e3182877F11. 3. Murphy MB, Moncivais K, Caplan et al,(2013): Mesenchymal Stem Cells: environmentally responsive therapeutics for regenerative medicine. Exp. Mol. Med. 45:e54.doi: 10.1038/emm 20.13.94. 4. Buchanan RM, Blashki D, Murphy MB (2014) Stem Cells therapy for regenerative medicine. Chem Eng Prog 110:55-58. 5. Hernigou P, Homma Y, Flouzat Lachaniette HC et al, (2013). Benefits of small volume and small syringe for bone marrow aspirations of Mesenchymal Stem Cells. Int. Orthop.37:2279-2287. doi.10.1007/s00264-013-2017-z. 6. Murphy MB, Blashki D, Buchanan RM et al, (2012): Adult and umbilical cord blood-derived Platelet-Rich Plasma for Mesenchymal Stem Cells proliferation, chemotaxis and cryo-preservation. Biomaterials 33: 5308-5316. doi. 10.1016/ j.biomaterials 20.12.04.007. 7. Pettine KA, Murphy MB, Suzuki RK, Sand TT,(2015):Percutaneous Injection of Autologous Bone Marrow Concetrate Cells significally reduces Lumbar Discogenic Paint through 12 months Stem Cells 33:146-56.doi.10.1002/stem.1845. 8. Tibiletti M, Kregar Velikonja N, Urban JOG, Fairbank JCT. : Disc Cell Therapies: critical issues. Eur.Spine J .2014:23:375-384.
Αρθρο του Melrose J., (2016)
O Μεσοσπονδύλιος Δίσκος αποτελεί μία κατασκευή η οποία σκοπό έχει να μεταφέρει τα βάρη του σώματος, με συνέπεια να υφίσταται εκφυλιστικές μεταβολές με την εξέλιξη της ηλικίας, περιοριζόμενης κατά συνέπεια της ικανότητάς του να κατανέμει την αξονική φόρτιση στην οποία υποβάλλεται, κατά ένα αποτελεσματικό τρόπο, με επακόλουθο τη πρόληψη Οσφυαλγίας.
Προληπτικές μελέτες για τη χορήγηση Μεσεγχυματικών Βλαστοκυττάρων σε Μεσοσπονδύλιους Δίσκους σκύλων και βοοειδών, κατέδειξαν εντυπωσιακά αποτελέσματα στην επιδιόρθωση βλαβών των Μεσοσπονδυλίων Δίσκων (ΜΔ). Στην εκτεταμένη μελέτη του ο Melrose J., πιστεύει ότι, ο συνδυασμός θεραπευτικών προσεγγίσεων με Βιοϋλικά και Μεσεγχυματικά Βλαστοκύτταρα, υπόσχεται σημαντική πρόοδο στην επιδιόρθωση των Μεσοσπονδυλίων Δίσκων στο εγγύς μέλλον.
Μelrose J. : Strategics in Regenerative Medicine for Ιntervertebral Disc repair using Mesenchymal Stem Cells and Bioscaffolds: Regen. Med. 2016, 11 :705-24.
Άρθρο των Carla Cunba and al, (2017)
Οι Carla Cunba and al, δημοσιεύουν τις παρατηρήσεις τους επί των κυτταρικών θεραπειών που αναπτύσσονται τελευταίως για την αναγέννηση του Μεσοσπονδυλίου Δίσκου (ΜΔ), με τη μεταμόσχευση κυττάρων του Μεσοσπονδυλίου Δίσκου (IVD Cells), ή Μεσεγχυματικών Βλαστοκυττάρων απευθείας στη θέση της βλάβης του δίσκου.
Είναι γνωστό ότι το «σκληρό» περιβάλλον που υφίσταται στο Μεσοσπονδύλιο Δίσκο, με τη μειωμένη παροχή υγρών και οξυγόνου, τα μεγάλα μηχανικά Stress και καταπονήσεις, δημιουργούν δυσκολότατες συνθήκες για επιβίωση κυττάρων και ιστών γενικότερα.
Στη μελέτη τους χορήγησαν αλλογενή Μεσεγχυματικά Βλαστοκύτταρα από το μυελό των οστών (BMMSCs) ενδοφλεβίως σε ποντίκια, στα οποία είχε προκληθεί εκφύλιση του Μεσοσπονδυλίου Δίσκου. Συνολικά, τα αποτελέσματα της έρευνας έδειξαν ότι υφίσταται ευεργετική δράση των συστηματικά χορηγούμενων MSCs σε Μεσοσπονδύλιους Δίσκους, στην αναγέννηση αυτών.
Carla Cunba and al, : Systemic Delivery of Bone Marrow Mesenchymal Stem Cells for In Situ Intervertebral Disc Regeneration, Stem Cells Transl. Med, 2017, Mar 6 (3) 1029-1039
Άρθρο των Migliorini F. and al, (2019)
Eπί του θέματος της χορήγησης αυτόλογων Μεσεγχυματικών Βλαστοκυττάρων (MSCs) δια ενέσεων, με το σκοπό της αναγέννησης του Μεσοσπονδυλίου Δίσκου (ΜΔ), συστηματική αναδρομική μελέτη της διεθνούς βιβλιογραφίας πραγματοποιήθηκε από τους Migliorini F. and al, και δημοσιεύθηκε το 2019.
Στη μελέτη τους οι συγγραφείς, περιέλαβαν μόνον άρθρα στα οποία αναφερόταν ότι γινόταν υποδορίως έγχυση ομολόγων MSCs στο Μεσοσπονδύλιο Δίσκο ανθρώπων. Οι συγγραφείς αξιολόγησαν τα ευρήματα και αποτελέσματα βάσει όλων των διεθνώς παραδεδειγμένων στατιστικών αναλυτικών μεθόδων. ‘Ολοι οι ασθενείς είχαν υποβληθεί προηγουμένως σε συντηρητική αντιμετώπιση της Οσφυαλγίας τους.
Οι παρατηρήσεις τους ήταν οι ακόλουθες :
Το Oswestry Disability Index (ΟDI) βελτιώθηκε από το επίπεδο της «σοβαρής ανικανότητας» σε εκείνο της «ελάχιστης» ανικανότητας, στο πρώτο χρόνο της παρακολούθησης. Το Visual Analogue Scale (VAS) μειώθηκε κατά 30% στον ίδιο χρόνο. Αναφέρθηκε μόνο μια περίπτωση εμφάνισης κήλης Μεσοσπονδυλίου Δίσκου. Δεν υπήρξαν παρενέργειες είτε από την αναρρόφηση είτε από τη χορήγηση των MSC.
Oι συγγραφείς στα συμπεράσματά τους, αναφέρουν ότι η χορήγηση MSCs, αποτελεί μία ασφαλή και εφικτή μέθοδο για την αναγέννηση του Μεσοσπονδυλίου Δίσκου, εφόσον αυτό γίνει στα αρχικά στάδια της εκφύλισής του. Άσχετα από τη πηγή λήψης των MSCs , έχει καταφανεί γενικά κλινική και ακτινολογική βελτίωση των ασθενών, όπως και εξαιρετικά χαμηλό ποσοστό επιπλοκών κατά τη παρακολούθησή τους, μετά τη χορήγηση των Μεσεγχυματικών Βλαστοκυττάρων.
Migliorini F. and al: Autogenic Mesenchymal Stem Cells for Intervertebral Disc Regeneration. Int. Orthop., 2019, April: 43(4)1027-1036.
Άρθρο των Wangler Sebastian and al, (2019)
Οι Wangler Sebastian and al, ερευνώντας τους πιθανούς παράγοντες που έχουν σχέση με την ιστική αναγέννηση του Μεσοσπονδυλίου Δίσκου, προέβησαν σε εκτεταμένη πειραματική μελέτη, η οποία δημοσιεύθηκε στο SPINE του Ιουλίου 2019. Ουσιαστικά, αντικειμενικός σκοπός της έρευνας ήταν να εκτιμηθεί η δράση των Μεσεγχυματικών Βλαστοκυττάρων (MSCs) :
α) επί των Τie 2-θετικών πολυδύναμων/πρόδρομων κυττάρων (progenitor) του Μεσοσπονδυλίου Δίσκου,
β) της επιβίωσης των κυττάρων του Μεσοσπονδυλίου Δίσκου, και
γ) του κυτταρικού πολλαπλασιασμού.
Δια το σκοπό αυτό, ανθρώπινα Mεσεγχυματικά Bλαστοκύτταρα απομονώθηκαν από αναρροφηθέντα οστικό μυελό (BMMSCs) και μετά από επεξεργασία χορηγήθηκαν σε ανθρώπινο ιστό που είχε ληφθεί από ανθρώπινο Μεσοσπονδύλιο Δίσκο.
Βασιζόμενοι στα αποτελέσματα της έρευνας, οι ερευνητές υποστήριξαν ότι τα Μεσεγχυματικά Βλαστοκύτταρα (MSCs) χορηγούμενα στο Μεσοσπονδύλιο Δίσκο, συμβάλλουν στην επιβίωση και στην αναγεννητική ικανότητα των κυττάρων του Μεσοσπονδυλίου Δίσκου, η οποία μπορεί να ενισχύεται από την υφιστάμενη ενδοκυττάριο επικοινωνία. Η χορήγηση MSCs στο Δίσκο μπορεί να αντιπροσωπεύσει μια δυνητική θεραπευτική στρατηγική, για να εμποδίσει την έναρξη της εκφυλιστικής διαδικασίας των Μεσοσπονδυλίων Δίσκων που είναι σε κίνδυνο, όπως συμβαίνει σε Μεσοσπονδύλιους Δίσκους σε επίπεδα παρακείμενα Σπονδυλοδεσίας, ή σε Δίσκους μετά από εμφάνιση Κήλης Δίσκου.
Wangler Sebastian et al, : Mesenchymal Stem Cells Homing into Intervertebral Discs. Enhances the Tie2-positive Progenitor Cell population, Prevents Cell Death and Induces a Proliferative Response. Spine, July 22, 2019, ( ahead of print)
Άρθρο των Markus Loibl and al, (2019)
Oι Markus Loibl and al (1) έκαναν εκτεταμένη αναδρομική μελέτη προκειμένου κα καταγράψουν τις αντίθετες απόψεις επάνω στη χρήση των Μεσεγχυματικών Βλαστοκυττάρων για την αντιμετώπιση της εκφύλισης των ανθρωπίνων Μεσοσπονδυλίων Δίσκων (ΜΔ).
Οι παρατηρήσεις των Μarkus Loibl and al (1) είναι οι ακόλουθες :
1. ΕΠΙΛΟΓΗ ΑΣΘΕΝΩΝ ΓΙΑ ΕΓΧΥΣΗ (MSCs) ΜΕΣΕΓΧΥΜΑΤΙΚΩΝ ΒΛΑΣΤΟΚΥΤΤΑΡΩΝ : Ανέτρεξαν σε 6 μελέτες (37-42) οι οποίες διερεύνησαν την αποτελεσματικότητα εγχύσεων MSC σε ασθενείς με εκφύλιση του Μεσοσπονδυλίου Δίσκου (DDD) και χρόνια Οσφυαλγία (LBP). Η μέση ηλικία των ασθενών στις μελέτες κυμαινόταν από 38 μέχρι 52 χρόνια. Στην ακτινολογική διερεύνηση, όλοι οι ασθενείς εμφάνισαν την ύπαρξη εστιακής βλάβης του ΜΔ σε ένα ή δύο επίπεδα της Οσφυϊκής Μοίρας της Σπονδυλικής Στήλης (ΟΜΣΣ). Η εκφύλιση του ΜΔ κατά τη κλίμακα Phirrmann, αναφέρεται στις περισσότερες μελέτες και κυμαίνεται από το ΙΙ έως το IV. Γενικά, όλοι οι ασθενείς είχαν υποβληθεί σε συντηρητική θεραπευτική αγωγή (φυσικοθεραπευτική και φαρμακευτική) για 3 έως 6 μήνες, η οποία απέτυχε να βελτιώσει τα συμπτώματά τους και θεωρήθηκε ότι είναι κατάλληλοι υποψήφιοι για να υποβληθούν σε έγχυση MSC. Πολύ μικρός αριθμός ασθενών αιτιάτο για ισχιαλγία. Δισκογραφήματα έγιναν στους περισσότερους ασθενείς για να επιβεβαιωθεί ο συμπτωματικός ΜΔ.
2. ΟΦΕΛΗΘΗΚΑΝ ΑΠΟ ΤΗ ΧΟΡΗΓΗΣΗ MSCs–ΜΕΣΕΓΧΥΜΑΤΙΚΩΝ ΒΛΑΣΤΟΚΥΤΤΑΡΩΝ Συνολικά 78 ασθενείς στους οποίους έγινε έγχυση MSC περιελήφθησαν στις 6 μελέτες και παρακολουθήθηκαν για 6 έως 72 μήνες. Σε αυτούς τους ασθενείς, διαπιστώθηκε σημαντική βελτίωση δύο δεικτών εκτίμησης του πόνου και της λειτουργικής ανικανότητας των πασχόντων, που είναι το Oswestry Disability Index (ODI) και το Visual Analogue Scale (VAS). H βελτίωση αυτή διαπιστώθηκε σε 51 από τους 78 ασθενείς, ποσοστό 65,4%. Στις περισσότερες μελέτες, το ύψος του Μεσοσπονδυλίου Δίσκου το οποίο εκτιμήθηκε από το MRI δεν βελτιώθηκε, ωστόσο διαπιστώθηκε βελτίωση κατά ένα βαθμό Phirrmann σε 8 ασθενείς στους 12 μήνες παρακολούθησης.
3. ΕΧΕΙ ΣΗΜΑΣΙΑ Η ΠΗΓΗ ΠΡΟΕΛΕΥΣΗΣ ΜΕΣΕΓΧΥΜΑΤΙΚΩΝ ΒΛΑΣΤΟΚΥΤΤΑΡΩΝ ; Στις εργασίες που μελέτησαν οι Markus Loibl and al, χρησιμοποιήθηκαν καλλιεργημένα Μεσεγχυματικά Κύτταρα από το μυελό των οστών (MSCs), από Λιπώδη Ιστό (ADS), από Συμπύκνωμα Κυττάρων του Μυελού των Οστών (ΒΜΜCs) και από Στρωματικά Ενδοθηλιακά Κύτταρα των Αγγείων (SVF) του λιπώδους ιστού. Τα κύτταρα του μυελού των οστών, σε δύο από τις μελέτες καλλιεργήθηκαν για να πολλαπλασιασθούν για 3 με 4 εβδομάδες προτού να χορηγηθούν, όπως και τα MSCs από το λιπώδη ιστό και τα ενδοθηλιακά στρωματικά κύτταρα των αγγείων του λιπώδους ιστού για 3 εβδομάδες Στη μελέτη τους οι Markus Loibl and al, αναφέρονται ακόμη σε μία άλλη μελέτη των Norienga et al, (47), οι οποίοι για οικονομικούς λόγους, χρησιμοποίησαν αλλογενούς προέλευσης Μεσεγχυματικά κύτταρα του μυελού των οστών (ΜSCs) χωρίς να έχει γίνει έλεγχος Ανοσοβιολογικής Ιστοσυμβατότητας. Στην μελέτη αυτή διαπιστώθηκε βελτίωση του πόνου (VAS) και της ανικανότητας (ODI) που άρχιζε να γίνεται εμφανής στους τρείς μήνες μετά την έγχυση των κυττάρων, σε ποσοστά ανάλογα εκείνων με τη χορήγηση αυτόλογων MSCs.
Ο αριθμός των εγχεόμενων κυττάρων (MSCs) κυμαινόταν από 10 μέχρι 60×10 ανά Μεσοσπονδύλιο Δίσκο (MD). Αναφέρεται ότι οι Pettine et al, (41) αντιμετώπισαν 26 ασθενείς με Οσφυαλγία, χορηγώντας συμπύκνωμα αυτόλογου μυελού των οστών (BMC) με παρακολούθηση των ασθενών το λιγότερο για 2 χρόνια (41). Αυτοί παρατήρησαν μεγαλύτερη και ταχύτερη μείωση των δεικτών ODI και VAS , όταν ο αριθμός των χορηγουμένων κυττάρων ήταν μεγαλύτερος από 2000 CFU-F/ml. Αυτό δείχνει ότι η αποτελεσματικότητα της χορήγησης (Transplantation) εξαρτάται από τη ποσότητα των MSCs.
Αντιθέτως, οι Kumar et al, (37), δεν βρήκαν να υπάρχει στατιστική διαφορά μεταξύ χαμηλής και υψηλής δόσης αυτολόγων MSCs, που λαμβάνονται από τον υποδόριο λιπώδη ιστό της κοιλιάς, όταν ο τελικός αριθμός των κυττάρων κυμαίνεται από 20×10 μέχρι 40×10
4. Η ΕΓΧΥΣΗ (Transplantation) MSC , ΕΙΝΑΙ ΜΙΑ ΑΣΦΑΛΗΣ ΔΙΑΔΙΚΑΣΙΑ ; Στις 6 εργασίες που μελετήθηκαν, δεν διαπιστώθηκαν σοβαρές παρενέργειες ή επιπλοκές. Ο Elabd et al, (38) σε πέντε ασθενείς στους οποίους έγινε ενδοδισκική έγχυση αυτόλογων Μεσεγχυματικών Βλαστοκυτάρων από το μυελό των οστών πολλαπλασιασμένων σε υποξικές συνθήκες με 5% επίπεδο οξυγόνου, δεν διαπίστωσε ανωμαλίες ή νεοπλασματικές εξεργασίες στις γειτονικές περιοχές κατά την επί 4-6 έτη παρακολούθηση με Μαγνητική Τομογραφία.
Βάσει των ανωτέρω οι Markus Loibl et al (1), έβγαλαν τα εξής συμπεράσματα :
(Α) Μεγάλη πρόοδος έχει γίνει στη προσπάθεια προσδιορισμού των καταλλήλων πηγών για MSCs, των κυτταρικών υποκατηγοριών και των πρωτοκόλλων καλλιέργειας και χορηγήσεων των MSCs, ώστε να προωθηθεί η κλινική επιτυχία της αναγέννησης του Μεσοσπονδυλίου Δίσκου δια της χορήγησης MSCs.
Αρκετές προ-κλινικές έρευνες έδειξαν ότι η θεραπεία, στηριζόμενη στη χορήγηση MSCs, αποτελεί μια αποτελεσματική μέθοδο για τη προώθηση της αναγέννησης του Δίσκου και επηρεασμό του πόνου. Οι κλινικές μελέτες έδειξαν ότι η χορήγηση MSCs είναι μια ασφαλής θεραπευτική μέθοδος σε ασθενείς με εκφύλιση του Μεσοσπονδυλίου Δίσκου (DDD), οι οποίοι αιτιώνται Οσφυαλγία τουλάχιστον για 6 μήνες, παρά τη συντηρητική θεραπευτική αγωγή, δεδομένου ωστόσο ότι ο ινώδης δακτύλιος είναι ακέραιος.
Αναλύοντας οι Markus Loibl et al, όλους τους ασθενείς των 6 κλινικών μελετών, παρατήρησαν ότι δεν ωφελήθηκαν όλοι το ίδιο από τη θεραπεία με τα MSCs, αποδεικνύοντας κατ΄αυτό το τρόπο ότι η επιλογή των ασθενών είναι ουσιαστική, δεδομένου ότι υπεισέρχονται ακόμη άγνωστοι παράγοντες.
Η ιδέα να χρησιμοποιούνται Μεσεγχυματικά Βλαστοκύτταρα (MSCs) για τη θεραπεία της Οσφυαλγίας είναι πολύ ελκυστική. Η διαδικασία είναι απλή, ελάχιστα επεμβατική και γίνεται απλώς μια ένεση μέσα στο Μεσοσπονδύλιο Δίσκο (ΜΔ). Πειραματικές εργασίες που έχουν γίνει σε ζώα, έχουν δώσει πολύ ενθαρρυντικά αποτελέσματα όσον αφορά την επιδιόρθωση του εκφυλισμένου Πηκτοειδούς Πυρήνα (ΠΠ) του Μεσοσπονδύλιου Δίσκου (ΜΔ), εντός ολίγων μηνών μετά την έγχυση. Κλινικές μελέτες επίσης έδειξαν μείωση του πόνου και σε μερικές περιπτώσεις και του επιπέδου εκφύλισης του ΜΔ κατά Phirrmann. Η βάση της υπόθεσης για τη χρήση των MSCs, είναι ότι η εκφύλιση του Μεσοσπονδυλίου Δίσκου (MΔ) είναι υπεύθυνη για την Οσφυαλγία. Οι μηχανισμοί, δια των οποίων οι εγχύσεις MSC μπορούν να μειώσουν το πόνο, εξαρτώνται από το «άθροισμα» επί μέρους παραγόντων όπως είναι : η εκφύλιση του ΜΔ που προκαλεί το πόνο και η επίδραση των Μεσεγχυματικών Βλαστοκυττάρων (MSCs) στο Μεσοσπονδύλιο Δίσκο( ΜΔ).
(Β) Οι Μεσοσπονδύλιοι Δίσκοι μπορεί να είναι ενδογενώς επώδυνοι, λόγω φλεγμονωδών διαδικασιών και μεταβολών στο Ph, που οδηγούν σε εκφυλιστικές μεταβολές, οι οποίες σε έρευνες στα πειραματόζωα φαίνεται να τροποποιούνται από τα MSCs, τα οποία είναι γνωστά για τις ανοσο-τροποποιητικές και αντι-φλεγμονώδεις δράσεις.
Οι παθολογικές μεταβολές μπορούν επίσης να επηρεάσουν τις τελικές σπονδυλικές πλάκες (Εnd Ρlates) και τα MSCs αναφέρεται ότι τροποποιούν το φλεγμονώδες περιβάλλον, το Ph και τη μειωμένη παροχή αίματος σε αυτή τη περιοχή. Τελικά, ο πόνος μπορεί να προκαλείται από μηχανική διαταραχή του επιπέδου κίνησης,όπως είναι η ιδιοδεκτικότητα (proprioception) και η εκφύλιση της σπονδυλικής διάρθρωσης (Facet).
Οι ενδοδισκικές εγχύσεις MSCs , θεωρείται ότι μπορεί να τροποποιήσουν αυτές τις πηγές έναρξης του πόνου, μέσω της επιδιόρθωσης και αναγέννησης του ιστού του ΜΔ, αποκαθιστώντας κατ΄αυτό τον τρόπο την εμβιομηχανική συμπεριφορά του ΜΔ, και των περιβαλλουσών σπονδυλικών ανατομικών δομών (22).
(Γ) Οι Markus Loibl et al, προβαίνουν ωστόσο σε ορισμένες περαιτέρω παρατηρήσεις. Δεδομένου ότι η ακτινολογική διερεύνηση με Μαγνητική Τομογραφία και ορισμένες κλινικές δοκιμασίες είναι τα μόνα μέσα για διάγνωση προκειμένου να γίνει η σωστή επιλογή ασθενούς, είναι φανερό ότι η επιλογή είναι δύσκολη. Εφόσον η θεραπεία με Μεσεγχυματικά Βλαστοκύτταρα (MSCs) θα βοηθήσει αυτούς τους ασθενείς των οποίων ο πόνος έχει σαν απαρχή την εκφύλιση του Μεσοσπονδυλίου Δίσκου (ΜΔ), οι αφετηρίες έναρξης των συμπτωμάτων, όπως είναι η διαταραχή του μηχανισμού του πόνου, η ευαισθητοποίηση του πόνου και οι μη ειδικοί ψυχολογικοί παράγοντες, δεν θα επηρεασθούν από τη χορήγηση MSCs.
Γενικά δεν υπάρχει συμφωνία όσον αφορά τη καλύτερη μέθοδο διάγνωσης και σύστημα κατηγοριοποίησης, προκειμένου να προσδιορισθούν οι καλύτεροι υποψήφιοι ασθενείς για να υποβληθούν σε θεραπεία για αναγέννηση του ΜΔ (22,29,43).
(Δ) Οι Μarkus Loibl et al , έθεσαν το ερώτημα εάν υπάρχει σαφής επιστημονική θέση (Clinical Evidence) για την αποτελεσματικότητα των θεραπειών με Μεσεγχυματικά Βλαστοκύτταρα (MSCs Therapies).
Προκειμένου να γίνει αξιόπιστη μελέτη όσον αφορά την αποτελεσματικότητα των κυτταρικών θεραπειών πρέπει να γίνουν τυχαιοποιημένες προοπτικές μελέτες σε μεγάλες ομάδες ασθενών. Οκτώ κλινικές δοκιμασίες είναι ήδη υπό εξέλιξη, χωρίς να έχουν ανακοινωθεί αποτελέσματα μέχρι τώρα.
Από τις μέχρι τώρα δημοσιευμένες εργασίες που αναφέρονται σε κλινικές μελέτες, με μικρό αριθμό ασθενών στους οποίους έγινε έγχυση Μεσεγχυματικών Βλαστοκυττάρων (MSCs) για τη θεραπεία εκφυλισμένου Μεσοσπονδυλίου Δίσκου (DDD), μόνο σε μία εργασία (47) δεν αναφέρθηκαν ευεργετικά αποτελέσματα από την έγχυση των MSCS για τη θεραπεία του Μεσοσπονδυλίου Δίσκου (ΙVD). Σε άλλες δημοσιεύσεις (37- 42) προτείνεται η χορήγηση MSCs σαν αιτιολογημένη μέθοδος θεραπείας για τον εκφυλισμένο ΜΔ, χωρίς ωστόσο να μπορεί να αποκλεισθεί ακόμη και σε αυτές τις μελέτες η Plecebo δράση.
Γενικότερα, μέχρι τώρα δεν υπάρχουν πολυκεντρικές μελέτες και οι δημοσιεύσεις περιλαμβάνουν μικρό αριθμό ασθενών. Επίσης τα πρωτόκολλα των κλινικών μελετών διαφέρουν μεταξύ τους ως προς πλείστες παραμέτρους, όπως είναι : τα κριτήρια επιλογής των ασθενών, οι επιλεχθείσες πηγές προέλευσης των MSCs, οι μέθοδοι χορήγησης (Transplantation) και οι μέθοδοι παρακολούθησης μετά τη χορήγηση των MSCs. Επιπλέον, στις κλινικές μελέτες συνήθως δεν περιλαμβάνονται ορισμένες ειδικές παράμετροι, όπως είναι το ποσοστό επιβίωσης
(Survival Rate) των εγχεόμενων MSCs και η εκτίμηση της βιολογικής δραστηριότητάς τους. Οι πιθανές παρενέργειες της χορήγησης MSCs έχουν διερευνηθεί, αλλά μέχρι τώρα δεν έχει αναφερθεί ειδική επιπλοκή. Σε μια μόνο εργασία (5) που έγινε σε εκφυλισμένο Μεσοσπονδύλιο Δίσκο κουνελιών, αναφέρεται ότι η διαφυγή κυττάρων μπορεί να προκαλέσει τη δημιουργία οστεοφύτων.
(Ε) Τίθεται το ερώτημα : Μπορούν τα Μεσεγχυματικά Βλαστοκύτταρα (MSCs) να παραμείνουν ζωντανά μετά την έγχυση μέσα στο Μεσοσπονδύλιο Δίσκο ;
Προκειμένου να είναι ικανά τα MSCs να επιτελέσουν τους σκοπούς για τους οποίους εγχέονται,τη διέγερση της μήτρας (matrix) του Μεσοσπονδυλίου Δίσκου (ΜΔ) και τη καταστολή της φλεγμονής, πρέπει να παραμείνουν ζωντανά στο περιβάλλον του ΜΔ. Αυτό σημαίνει ότι απαιτείται να υπάρχει επαρκής παροχή θρεπτικών ουσιών, ιδιαιτέρως γλυκόζης, διότι όπως και τα ιθαγενή κύτταρα του δίσκου έτσι και τα MSCs είναι γλυκολυτικά και πεθαίνουν γρήγορα, εάν η γλυκόζη (και όχι το Ο2) αφαιρεθεί.
Η αποτελεσματική αφαίρεση του γαλακτικού οξέως (Lactic Αcid) του κύριου προϊόντος μεταβολισμού της γλυκόλυσης, είναι επίσης ουσιαστικός παράγοντας, δεδομένου ότι όξυνση του Ph, που διαπιστώθηκε σε εκφυλισμένους Μεσοσπονδύλιους Δίσκους, είναι επιβλαβής στη κυτταρική δραστηριότητα και στην επιβίωση των MSCs και των ιθαγενών (αυτόχθονων) δισκικών κυττάρων.
Ο φυσιολογικός ΜΔ είναι μεγάλος και στερείται αγγείων, γιαυτό και οι θρεπτικές ουσίες που είναι απαραίτητες για την επιβίωση των αυτόχθονων κυττάρων του ΜΔ, παρέχονται από τα αιμοφόρα αγγεία, στα όρια του σπονδυλικού σώματος με τον ΜΔ. Οι συγκεντρώσεις των θρεπτικών ουσιών στον ΜΔ , εξαρτώνται από την ισορροπία που υφίσταται μεταξύ των παρεχομένων θρεπτικών ουσιών και των κυτταρικών απαιτήσεων. Κατά συνέπεια, οι συγκεντρώσεις θρεπτικών ουσιών εντός του ΜΔ μειώνονται, εξαρτώμενες από την απόσταση που υπάρχει από την αιματική παροχή. Αυτό σημαίνει ότι ο ΜΔ μπορεί να στηρίζει ένα περιορισμένο αριθμό κυττάρων προτού οι θρεπτικές συγκεντρώσεις στο κέντρο του ΜΔ γίνουν τόσο χαμηλές, ώστε να είναι δύσκολο να διατηρηθεί η βιωσιμότητά τους. Έτσι, η υποστηριζόμενη κυτταρική πυκνότητα συσχετίζεται αντίστροφα με το ύψος του ΜΔ.
Η παροχή θρεπτικών ουσιών περιορίζεται στους εκφυλισμένους ΜΔ, με συνέπεια να είναι η κυτταρική πυκνότητα χαμηλότερη εκείνης των φυσιολογικών μεσοσπονδυλίων δίσκων, διότι τα κύτταρα πεθαίνουν μέχρι να μειωθεί ο αριθμός τους τόσο, ώστε να μπορεί να ανταποκριθεί στη μειωμένη παροχή θρεπτικών ουσιών.
Η χορήγηση MSCs θα διαταράξει περαιτέρω τη τροφική ισορροπία, δεδομένου ότι η αύξηση του αριθμού των κυττάρων θα αυξήσει τη ζήτηση θρεπτικών ουσιών και θα επακολουθήσει κυτταρικός θάνατος, διότι τα εγχεόμενα MSCs θα ανταγωνίζονται τα παραμένοντα ζώντα αυτόχθονα κύτταρα του ΜΔ στις παρεχόμενες θρεπτικές ουσίες. Είναι άγνωστο αν θα επιβιώσουν καλύτερα τα μεταμοσχευόμενα ή τα αυτόχθονα κύτταρα και επί του παρόντος δεν υπάρχουν διαγνωστικές τεχνικές για να γίνει ο σχετικός έλεγχος.
Ζ) Τίθεται ένα ακόμη ερώτημα : Τα Μεσεγχυματικά Βλαστοκύτταρα (MSCs) που θα επιβιώσουν, μπορούν να δράσουν επαρκώς στο Μεσοσπονδύλιο Δίσκο (ΜΔ) ;
Οι γλυκοζαμινογλυκάνες (GAGs) της Αγγρεκάνης (aggrecan) είναι υπεύθυνες για τη διατήρηση της ενυδάτωσης του Μεσοσπονδυλίου Δίσκου (ΜΔ) και τη διατήρηση του ύψους του. Η μείωση των GAGs αποτελεί ένα από τα πρώτα σημάδια της εκφύλισης του Μεσοσπονδυλίου Δίσκου (DDD). Για αυτό το λόγο, η αποκατάσταση της συγκέντρωσης GAGs είναι το απαιτούμενο για τη διόρθωση του ΜΔ. Αναφέρεται ότι η ποσότητα GAGs που παράγεται από τα MSCs , ποικίλλει σημαντικά μεταξύ των ζωϊκών ειδών, τη πηγή των MSCs και τις τεχνικές καλλιέργειας και παρασκευής.
Δεδομένου ότι η συγκέντρωση GAGs στο Πηκτοειδή Πυρήνα φυσιολογικού Μεσοσπονδυλίου Δίσκου είναι περί τα 70 mg/ml και ο φυσιολογικός ανθρώπινος Μεσοσπονδύλιος Δίσκος δεν μπορεί να υποστηρίζει περισσότερο από περίπου 3 εκατομμύρια κύτταρα/ml, οι υπολογισμοί δείχνουν ότι θα χρειασθούν δεκαετίες για να αποκατασταθεί το 25% του ιστού του ΜΔ και της aggrecan που χάθηκε στον ασθενή, δια της εγχύσεως (Implantation) MSCs.
Η βραδύτατη αποκατάσταση του ΜΔ με MSCs μπορεί να ερμηνεύσει τα ευρήματα, ότι η ημίσεια ζωή (Half Life) της aggrecan των ανθρωπίνων ΜΔ, είναι 4 μέχρι 6 χρόνια και ότι τα MSCs παράγουν GAGs σε ποσότητα γύρω στο 20% με 30% εκείνης των κυττάρων του φυσιολογικού Πηκτοειδούς Πυρήνα (ΝΡ).
(Η) Οι Markus Loibl et al, στην αναδρομική μελέτη έθεσαν το ερώτημα : Εναλλακτικά, είναι σε θέση τα επιβιώσαντα MSCs να διεγείρουν τα αυτόχθονα κύτταρα του ΜΔ (IVD) για να διορθώσουν τον ΜΔ (IVD) ή να μειώσουν τη παραγωγή φλεγμονωδών παραγόντων ;
Οι εκφυλισμένοι Μεσοσπονδύλιοι Δίσκοι έχουν χαμηλή πυκνότητα κυττάρων. Τα κύτταρα του Δίσκου επιπλέον, παράγουν GAGs αργά, λόγω του κακού περιβάλλοντος και διότι πολλά κύτταρα του Πηκτοειδούς Πυρήνα έχουν γεράσει. Παράγοντες προερχόμενοι από τα εμφυτευμένα MSCs , αν τα κύτταρα επιβιώσουν σε σχετικώς επαρκή μεγάλη πυκνότητα, μπορούν να περιορίσουν τη φλεγμονή, να βελτιώσουν το μικρο-περιβάλλον και να μειώσουν το πόνο. Μπορεί επίσης να δημιουργήσουν παράγοντες οι οποίοι διεγείρουν τη παραγωγή GAGs από τον εναπομείναντα μικρό αριθμό κυττάρων του Πηκτοειδούς Πυρήνα.
Αυτό όμως θα συμβεί με κόστος καθότι τα διεγερμένα κύτταρα απαιτούν περισσότερες διατροφικές ουσίες, διαταράσσοντας πάλι την ισορροπία μεταξύ της διατροφικής παροχής και της ζήτησης, διακινδυνεύοντας αυξημένο θάνατο των κυττάρων. Προκαλεί προβληματισμό, στο αν τα μεταμοσχευόμενα (Implanted) κύτταρα θα επιβιώσουν σε οποιαδήποτε σημαντική πυκνότητα, εντός των εκφυλισμένων Μεσοσπονδυλίων Δίσκων, που έχουν ήδη χάσει μέρος του αυτόχθονου κυτταρικού πληθυσμού λόγω της περιορισθείσης διατροφικής παροχής.
(Θ) Γενικό Συμπέρασμα
Οι Μarkus Loibl et al, πηγαίνοντας αρκετά διεξοδικά διαμέσου πολλών δημοσιεύσεων σχετικά με τη χορήγηση Μεσεγχυματικών Βλαστοκυττάρων (MSCs) κατέληξαν στα εξής :
Μεταξύ άλλων τύπων κυττάρων, τα Μεσεγχυματικά Βλαστοκύτταρα (MSCs) έχουν χορηγηθεί δια ενέσεων για τη θεραπεία του εκφυλισμένου Μεσοσπονδυλίου Δίσκου (DDD). Παρά τις υποσχόμενες προ-κλινικές μελέτες, οι κλινικές μελέτες και τα αποτελέσματά τους είναι ανεπαρκείς, γιαυτό και απαιτούνται να γίνουν πολυκεντρικές, προοπτικές, τυχαιοποιημένες μελέτες.
Οπωσδήποτε, τα MSCs έχουν μεγάλες αναγεννητικές δυνατότητες, που οφείλονται στα χαρακτηριστικά του πολλαπλασιασμού τους, στην αναβολική ικανότητά τους και στις ιδιότητες που έχουν για τροποποίηση της φλεγμονής.
Το κύριο πρόβλημα που πρέπει να υπερνικηθεί για να είναι επιτυχής η κυτταρική θεραπεία του Μεσοσπονδυλίου Δίσκου (IVD) είναι το «σκληρό» μικρο-περιβάλλον των Μεσοσπονδυλίων Δίσκων (IVDs) το οποίο περιορίζει τη ζωτικότητα και τη λειτουργικότητα των εγχεόμενων MSCs. Ωστόσο, οι σύγχρονες προσπελάσεις του προβλήματος, στις οποίες περιλαμβάνονται αναδυόμενες τεχνικές στις γονιδιωματικές θεραπείες έχουν τη δυνατότητα να ετοιμάσουν MSCs για επιβίωση μέσα στους Μεσοσπονδύλιους Δίσκους, ωθώντας περαιτέρω τις MSCs θεραπείες.
1. Markus Loibl and al, : Controversies in Regenerative Medicine: Should Intervertebral Disc Degeneration be Treated with Mesenchymal Stem Cells ? JOR Spine, 25 Jan.2019, Vol.2, Issue 1, e-1043.
2. Jones EA, Yang XB. Mesenchymal Stem Cells, and their future in bone repair. Int. J. Adv Rheumatol.2005: (3):15-21.
3. Kumar H, Ha D-H, Lee E-J et al: Safety and tolerability of intradiscal implantation of combined autologous andipose-derived Mesenchyumal Stem Cells and Hyaluronic Acid in patients with chronic discogenic low back pain: 1 year follow-up of a phase I study: Stem Cells Res.Ther.2017:8:262/doi.org/10.1186/s13287-017-0710-3.
4. Comella K, Silbert R, Parlo M,: Effects of the intradiscal implantation of stromal vascular fraction plus Platelet-Rich Plasma in patients with degenerative disc disease. J.Transl.Med.2017:15:12.
5. Noriega DC, Ardura F, Hernandez-Ramajo R, et al: Intervertebral disc repair by allogenic Mesenchymal Bone Marrow Cells: a randomized controlled trial. Transplantation. 2017:101:1945-1951.doi.org/10.1097/TP.0000000000001484.
6. Elabd C, Centeno Cj, Schultz JR, Lutz G, Ichim T,Silva Fj.: Intra-discal injection of autologous, hypoxic cultured bone marrow-derived mesenchymal stem cells in five patients with chronic lower back pain: a long term safety and feasibility study. J Transl Med.2016: 14:253.
7. Pettine KA, Murphy MB, Suzuki RK, Sand TT. : Percutaneous Injection of autologous bone marrow concentrate cells significantly reduces lumbar discogenic pain through 12 months: autologous bmc injection reduces discogegnic pain. Stem Cells. 2015 :33: 146-156.
8. Orozco L, Soler R, Morera C, Alberca M, Sanchez A, Garcia-Sancho J: Intervertebral disc repair by autologous Mesenchymal bone marrow cells: a pilot study. Transplantation. 2011:92:822-828.
9. Sakai D, Andersson GBJ, : Stem Cell therapy for Intervertebral disc degeneration: obstacles and solutions. Nat. Rev. Rheumatol. 2015:11:243-256.
10. Tibiletti M, Kregan Velikonja N, Urban JPG, Fairbank JCT: Disc Cell therapies: critical issues Eur. Spine J. 2014:23:375-384.
11. Carvalho C, Caetano JM, Cunha L, Rebouta P, Kaptchuck Tj, Kirsch J.: Open-label placebo treatment in chronic low back pain: a randomized controlled trial. Pain 2016: 157: 2766-2772.
12. Haufe SM, Mork AR: Intradiscal injection of hematopoetic Stem Cells in an attempt to rejuvenate the intrtervertebral discs. Stem Cells Dev. 2006: 15: 316-137.
13. Vadala GA, Sowa G, Hubert M, Gilbertson LG, Denaro V, Kang JD, : Mesenchymal Stem Cells injection in degenerated intervertebral disc: cell leakage may induce osteophyte formation. J. Tissue Eng Regen Med. 2012:6: 348-355.
Συντμήσεις – Αποδόσεις όρων
ΑDS……………………………………………………….Λιπώδης Ιστός
ADCs……………………………………………………..Μεσεγχυματικά Βλαστοκύτταρα από Λιπώδη Ιστό
AF(Annular Fibrosus)……………………………..ΙΔ (Ινώδης Δακτύλιος)
ΑGGRECAN……………………………………………Αγγρεκάνη
BIO-degredable………………………………….Βιοδιασπώμενο
ΒΜΑ (Bone Marrow Aspirate)………………..Aναρρόφηση Οστικού Μυελού
BMC(Bone Marrow Concetrate)…………….Συμπύκνωμα Μυελού των Οστών
BMLs (Bone Marrow Lesions)…………………Βλάστες του Οστικού Μυελού
ΒΜΜSCs………………………………………………..Μεσεγχυματικά Βλαστοκύτταρα από το Μυελό των Οστών
Bone Matrix ………………………………………….Οστική Μήτρα
Bone Remodeling ………………………………….Οστικός Ανασχηματισμός
CFU-F/MSC…………………………………………….Κύτταρα ανά κυβικό εκατοστό
DDD (Degenerative Disc Disease)…………..Εκφύλιση Μεσοσπονδυλίου Δίσκου
End Plate……………………………………………….Tελική Σπονδυλική Πλάκα
Facet………………………………………………………Σπονδυλική Διάρθρωση
GAGs (Glycosaminoglucanes)…………………Γλυκοζαμινογλυκάνες
Genomics……………………………………………….Γονιδιωματική
GTE (Cartilage Tissue Enginnering)……….. Ιστική Αναπαραγωγή Χόνδρου
IVDs (Intervertebral Disc)………………………..ΜΔ (Μεσοσπονδύλιος Δίσκος)
LBP (Low Back Pain)………………………………..Χρόνια Οσφυαλγία
Ml…………………………………………………………..Κυβικό εκατοστό (κ.εκ.)
MRΙ (Investigation)………………………………….Μαγνητική Τομογραφία
ΜSCs……………………………………………………….Μεσεγχυματικά Βλαστοκύτταρα
NP (Nucleus Pulposus)……………………………..ΠΠ (Πηκτοειδής Πυρήνας)
ΟΜΣΣ ……………………………………………………..Οσφυϊκή Μοίρα της Σπονδυλικής Στήλης
ODI………………………………………………………….Oswestry Disability Index
Placebo……………………………………………………Εικονικό φάρμακο
Progenitor Cells ……………………………………..Πρόδρομα Πολυδύναμα Κύτταρα
Proprioception…………………………………………Ιδιοδεκτικότητα
PRP (Platelet-Rich Plasma)………………………Πλάσμα Πλούσιο σε Αιμοπετάλια
Survival Rate…………………………………………..Ποσοστό επιβίωσης
TNC (Total Nucleated Cell)………………………Eμπύρηνα Κύτταρα
Transplantation ………………………………………Μεταμόσχευση
VAS………………………………………………………….Visual Analogue Scale
BMI (Body Mass Index)……………………………ΔΜΣ (Δείκτης Μάζας Σώματος) = Bάρος(kg)/Yψος 2(m) – ορίζεται ως το Βάρος σε κιλά διαιρούμενο με το τετράγωνο του ύψους σε μέτρα
Classification
Phirrmann Score (5 Levels) – Aφορά την εκφύλιση Μεσοσπονδυλίου Δίσκου
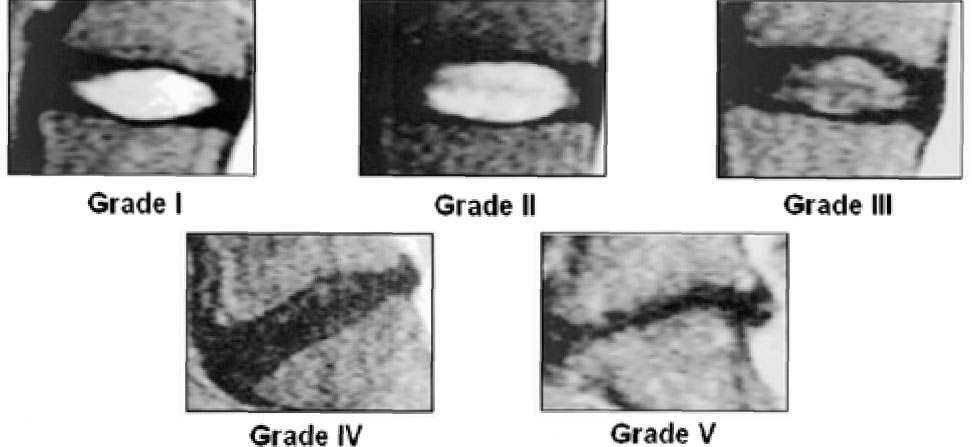
| Grade I | Homogeneous, bright white |
| Grade II | Inhomogeneous or without horizontal bands |
| Grade II | Inhomogeneous, gray |
| Grade IV | Inhomogeneous, gray to black |
| Grade V | Inhomogeneous, black |
Reference
Pfirrmann CW, Metzdorf A, Zanetti M etal.: Magnetic Resonance Classification of Lumbar Intervertebral Disc Degeneration. Spine. 2001; 26 (17): 1873-8. Pubmed citation
Modic: Αφορά τις Αλλοιώσεις των Μεσοσπονδυλίων Δίσκων
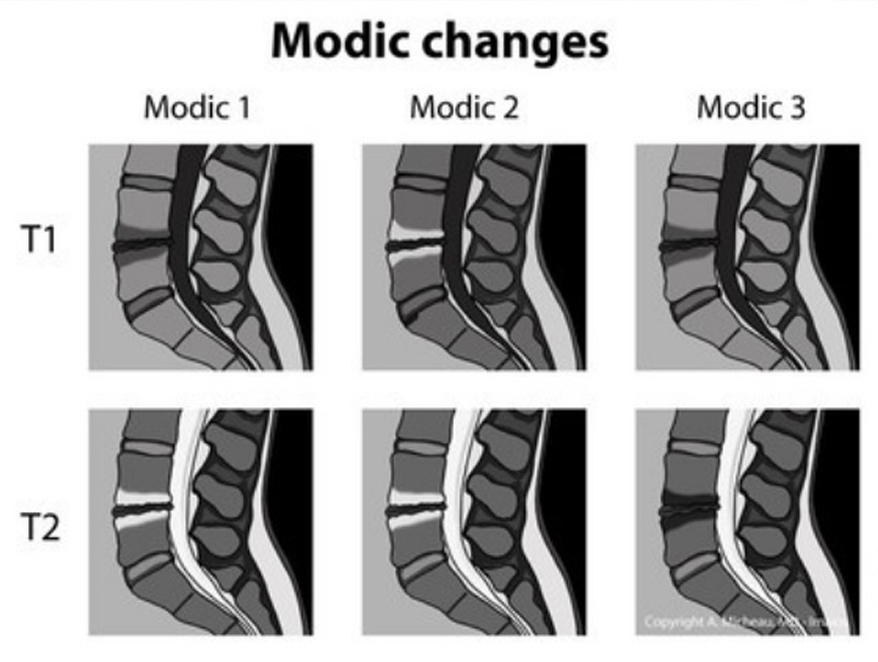
| Τύπος Ι : | Οστικό Οίδημα & αυξημένη Αγγειοβρίθεια |
| Τύπος ΙΙ : | Αντικατάσταση του Μυελού των Οστών από λίπος |
| Τύπος ΙΙΙ : | Υποχόνδρια Οστική Σκλήρυνση και ρωγμές στις Τελικές Σπονδυλικές Πλάκες |
Reference
Modic, MT, Steinberg, PM, Ross, JS, Masaryk, TJ, and Carter, JR.
Degenerative Disk Disease: Assessment of changes in Vertebral BoneMarrow with MR imaging.
Radiology. 1988; 166: 193–199
